Publication : Généthon contribue à clarifier un mécanisme moléculaire du dysfonctionnement de la mitochondrie dans la Dystrophie de Duchenne
Les essais cliniques de thérapie génique pour la Dystrophie de Duchenne (DMD) ont apporté des résultats encourageants, mais le bénéfice thérapeutique des patients traités reste insatisfaisant.
« Pour progresser encore davantage, il est nécessaire de mieux comprendre la physiopathologie de la maladie » déclare David Israeli.
« La DMD se caractérise par une fragilité des fibres musculaires, due à l’expression anormale de la dystrophine, dont une fonction principale est la stabilisation mécanique des muscles squelettiques mais aussi cardiaques ». David précise que « la dystrophine est une protéine de grande taille et de grande complexité qui a de nombreuses interactions moléculaires et des fonctions biologiques qui dépassent son rôle de stabilisateur mécanique des myofibres ».
L’objet des recherches menées par Ai Vu Hong sous la direction d’Isabelle Richard et de David Israeli est d’éclaircir les mécanismes de dysfonctionnement mitochondrial dans la DMD. Depuis de nombreuses années, il a été décrit que la perturbation de l’homéostasie du calcium est l’élément principal permettant de comprendre le dysfonctionnement mitochondrial dans la DMD.
Les résultats obtenus dans l’étude de Ai Vu Hong apportent un éclairge nouveau sur ce point. « Nous avons récemment constaté que, dans le muscle DMD, l’expression d’un microARN (miR-379), la sous-expression de protéines ayant un lien avec la mitochondrie (EIF4G2 et DAPIT), la diminution de la production d’ATP, peuvent se conjuguer à l’entrée massive de Ca2+ dans la cellule (Sanson et al.2020) http://www.nature.com/articles/s41598-020-66016-7 L’augmentation des radicaux libres et le stress oxydatif qui en découlent, entrainent des dommages dans les mitochondries et une dégénérescence des myofibres » précise David Israeli.
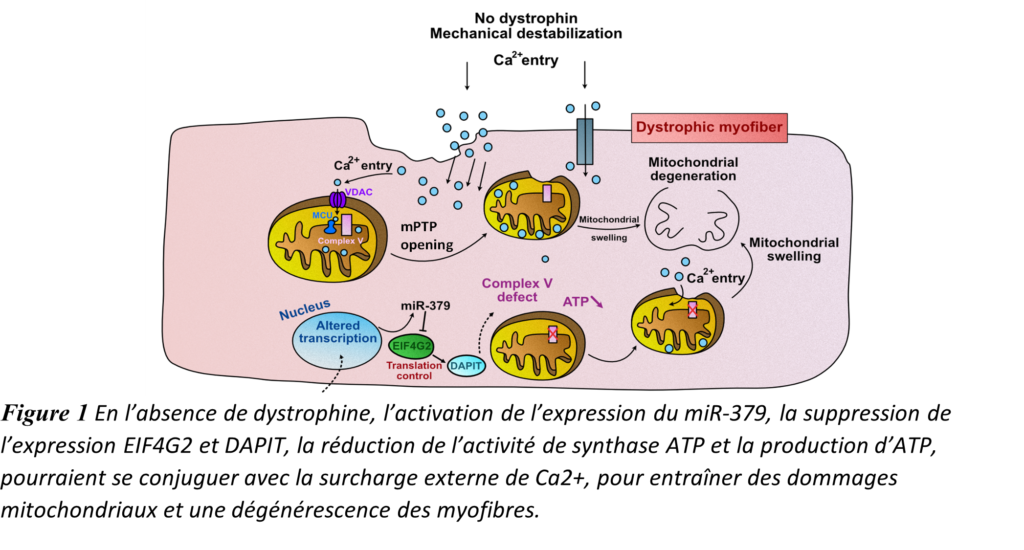
Le miRNA-379 fait partie comme de nombreux autres mi-RNAs du « cluster Dlk1-Dio3 miRNAs » dont une vingtaine sont dérégulés dans la DMD (Jeanson-Leh et al.2014) https://pubmed.ncbi.nlm.nih.gov/25194663/ . Ai vu Hong a montré que, de façon similaire au miRNA-379, d’autres mi-RNAs du même cluster Dlk1-Dio3 sont également impliqués dans la répression de la production d’énergie dans la mitochondrie. Il propose donc un modèle actualisé du dysfonctionnement mitochondrial dans DMD (Figure2).
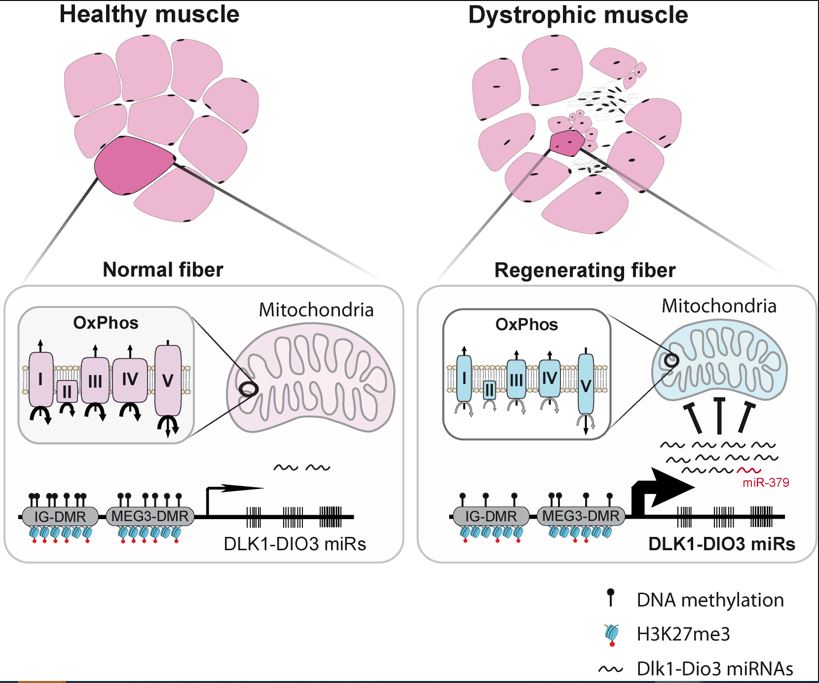
En résumé, cette publication permet de définir plus clairement un mécanisme fondamental de la mitochondrie dans la dystrophie musculaire de Duchenne.
En savoir plus
Vu Hong A, Bourg N, Sanatine P, Poupiot J, Charton K, Gicquel E, Massourides E,Spinazzi M, Richard I, Israeli D. October 21, 2022.

